1. Grundlæggende viden (hvis du vil se den eksperimentelle del, skal du overføre direkte til anden del)
Som en afledt reaktion af konventionel PCR overvåger realtids-PCR hovedsageligt ændringen af mængden af amplifikationsprodukt i hver cyklus af PCR-amplifikationsreaktionen i realtid gennem ændringen af fluorescenssignalet og analyserer startskabelonen kvantitativt gennem forholdet mellem ct-værdien og standardkurven.
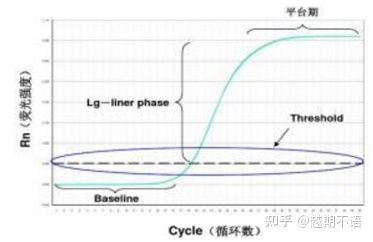
De specifikke data for RT-PCR erbaseline, fluorescensgrænseogCt værdi.
| baseline: | Fluorescensværdien for den 3.-15. cyklus er basislinjen (baseline), som er forårsaget af en lejlighedsvis fejl i målingen. |
| Tærskel (tærskel): | Refererer til fluorescensdetektionsgrænsen indstillet på en passende position i den eksponentielle vækstregion af amplifikationskurven, generelt 10 gange standardafvigelsen af basislinjen. |
| CT værdi: | Det er antallet af PCR-cyklusser, når fluorescensværdien i hvert reaktionsrør når tærsklen. Ct-værdien er omvendt proportional med mængden af initial skabelon. |
Almindelige mærkningsmetoder for RT-PCR:
| metode | fordel | mangel | anvendelsesområde |
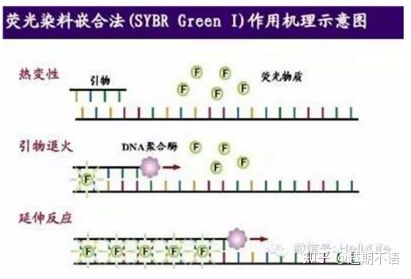
| SYBR GrønⅠ | Bred anvendelighed, følsom, billig og praktisk | Primerkravene er høje, tilbøjelige til ikke-specifikke bånd | Den er velegnet til kvantitativ analyse af forskellige målgener, forskning i genekspression og forskning i transgene rekombinante dyr og planter. |
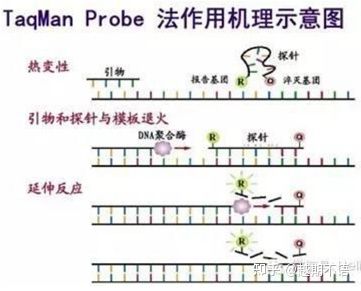
| TaqMan | God specificitet og høj repeterbarhed | Prisen er høj og kun egnet til specifikke mål. | Patogendetektion, lægemiddelresistens genforskning, lægemiddeleffektivitetsvurdering, diagnosticering af genetiske sygdomme. |
| molekylært fyrtårn | Høj specificitet, fluorescens, lav baggrund | Prisen er høj, den er kun egnet til et bestemt formål, designet er svært, og prisen er høj. | Specifik genanalyse, SNP-analyse |
2. Eksperimentelle trin
2.1 Om forsøgsgrupperingen- der skal være flere brønde i gruppen, og der skal være biologiske gentagelser.
| ① | Blank kontrol | Bruges til at detektere cellevækststatus i eksperimenter |
| ② | Negativ kontrol siRNA (ikke-specifik siRNA-sekvens) | Demonstrer specificiteten af RNAi-handling.siRNA kan inducere uspecifik stressrespons ved en koncentration på 200nM. |
| ③ | Transfektionsreagenskontrol | Udeluk toksiciteten af transfektionsreagenset til cellerne eller virkningen på ekspressionen af målgenet |
| ④ | siRNA mod målgenet | Slå ekspressionen af målgenet ned |
| ⑤ (valgfrit) | positiv siRNA | Bruges til at fejlfinde eksperimentelle system- og driftsproblemer |
| ⑥ (valgfrit) | Fluorescerende kontrol siRNA | Effektiviteten af celletransfektion kan observeres med et mikroskop |
2.2 Principper for primerdesign
| Amplificeret fragmentstørrelse | Gerne ved 100-150bp |
| Primer Længde | 18-25 bp |
| GC indhold | 30%-70%, fortrinsvis 45%-55% |
| Tm værdi | 58-60 ℃ |
| Sekvens | Undgå T/C kontinuerlig;A/G kontinuerlig |
| 3 ender sekvens | Undgå GC rig eller AT rig;den terminale base er fortrinsvis G eller C;det er bedst at undgå T |
| Komplementaritet | Undgå komplementære sekvenser på mere end 3 baser i primeren eller mellem to primere |
| Specificitet | Brug blastsøgning til at bekræfte primerspecificitet |
①SiRNA er artsspecifik, og sekvenserne af forskellige arter vil være forskellige.
②SiRNA er pakket i frysetørret pulver, som kan opbevares stabilt i 2-4 uger ved stuetemperatur.
2.3 Værktøj eller reagenser, der skal forberedes på forhånd
| Primer (intern reference) | Inklusiv to frem og tilbage |
| Primere (målgen) | Inklusiv to frem og tilbage |
| Target Si RNA (3 strimler) | Generelt vil virksomheden syntetisere 3 strimler og derefter vælge en af de tre ved RT-PCR |
| Transfektionssæt | Lipo2000 osv. |
| RNA Rapid Extraction Kit | Til RNA-ekstraktion efter transfektion |
| Hurtigt omvendt transskriptionssæt | til cDNA-syntese |
| PCR amplifikationskit | 2×Super SYBR Grøn qPCR Master Mix |
2.4 Med hensyn til de spørgsmål, der skal lægges vægt på i de specifikke eksperimentelle trin:
①siRNA-transfektionsproces
1. Til udpladning kan du vælge 24-brønds plade, 12-brønds plade eller 6-brønds plade (den gennemsnitlige RNA-koncentration foreslået i hver brønd i en 24-brønds plade er ca. 100-300 ng/uL), og den optimale transfektionstæthed af celler er op til 60 %-80 % eller deromkring
2. Transfektionstrinene og specifikke krav er strengt i overensstemmelse med instruktionerne.
3. Efter transfektion kan prøver indsamles inden for 24-72 timer til mRNA-detektion (RT-PCR) eller proteindetektion inden for 48-96 timer (WB)
② RNA-ekstraktionsproces
1. Undgå kontaminering med eksogene enzymer.Det omfatter hovedsageligt at bære masker og handsker strengt;ved hjælp af steriliserede pipettespidser og EP-rør;vandet brugt i forsøget skal være RNase-frit.
2. Det anbefales at gøre to gange som foreslået i kittet til hurtig ekstraktion, hvilket virkelig vil forbedre renheden og udbyttet.
3. Spildvæsken må ikke røre RNA-søjlen.
③ RNA kvantificering
Efter at RNA'et er ekstraheret, kan det kvantificeres direkte med Nanodrop, og minimumsaflæsningen kan være så lav som 10ng/ul.
④Omvendt transkriptionsproces
1. På grund af den høje følsomhed af RT-qPCR bør der laves mindst 3 parallelle brønde for hver prøve for at forhindre, at den efterfølgende Ct bliver for forskellig, eller SD'en er for stor til statistisk analyse.
2. Frys og optø ikke Master mix gentagne gange.
3. Hvert rør/hul skal udskiftes med en ny spids!Brug ikke konstant den samme pipettespids til at tilføje prøver!
4. Filmen fastgjort til 96-brøndspladen efter tilsætning af prøven skal glattes med en plade.Det er bedst at centrifugere, før det sættes på maskinen, så væsken på rørvæggen kan strømme ned og fjerne luftbobler.
⑤ Fælles kurveanalyse
| Ingen periode med logaritmisk vækst | Muligvis høj koncentration af skabelon |
| Ingen CT-værdi | Forkerte trin til detektering af fluorescerende signaler; nedbrydning af primere eller prober – dens integritet kan påvises ved PAGE-elektroforese; utilstrækkelig mængde skabelon; nedbrydning af skabeloner – undgåelse af introduktion af urenheder og gentagen frysning og optøning i prøveforberedelse; |
| Ct>38 | Lav forstærkningseffektivitet;PCR-produktet er for langt;forskellige reaktionskomponenter nedbrydes |
| Lineær forstærkningskurve | Prober kan blive delvist nedbrudt ved gentagne fryse-optøningscyklusser eller langvarig udsættelse for lys |
| Forskellen i dobbelte huller er særlig stor | Reaktionsopløsningen er ikke fuldstændig smeltet, eller reaktionsopløsningen er ikke blandet;PCR-instrumentets termiske bad er forurenet af fluorescerende stoffer |
2.5 Om dataanalyse
Dataanalysen af qPCR kan opdeles i relativ kvantificering og absolut kvantificering.For eksempel, celler i behandlingsgruppen sammenlignet med celler i kontrolgruppen,
Hvor mange gange X-genets mRNA ændres, dette er relativ kvantificering;i et vist antal celler, X-genets mRNA
Hvor mange kopier der er, dette er absolut kvantificering.Normalt er det, vi bruger mest i laboratoriet, den relative kvantitative metode.Som regel,2-ΔΔct metodenbruges mest i eksperimenter, så kun denne metode vil blive introduceret i detaljer her.
2-ΔΔct metode: Det opnåede resultat er forskellen i ekspressionen af målgenet i forsøgsgruppen i forhold til målgenet i kontrolgruppen.Det kræves, at amplifikationseffektiviteten af både målgenet og det interne referencegen er tæt på 100 %, og den relative afvigelse bør ikke overstige 5 %.
Beregningsmetoden er som følger:
Δct kontrolgruppe = ct værdi af målgen i kontrolgruppe – ct værdi af intern referencegen i kontrolgruppe
Δct forsøgsgruppe = ct værdi af målgenet i forsøgsgruppen – ct værdi af det interne referencegen i forsøgsgruppen
ΔΔct=Δct eksperimentel gruppe-Δct kontrolgruppe
Beregn endelig multiplum af forskellen i udtryksniveau:
Skift fold=2-ΔΔct (svarende til excel-funktionen er POWER)
Relaterede produkter:
Indlægstid: 20. maj 2023