Udgangsmateriale: RNA
Kvantitativ revers transkriptions-PCR (RT-qPCR) er en eksperimentel metode, der anvendes i PCR-eksperimenter med RNA som udgangsmateriale.I denne metode transskriberes totalt RNA eller messenger-RNA (mRNA) først til komplementært DNA (cDNA) ved hjælp af revers transkriptase.Efterfølgende blev en qPCR-reaktion udført under anvendelse af cDNA'et som skabelon.RT-qPCR er blevet brugt i en række molekylærbiologiske applikationer, herunder genekspressionsanalyse, RNA-interferensvalidering, microarray-validering, patogendetektion, genetisk testning og sygdomsforskning.
Et-trins og to-trins metoder til RT-qPCR
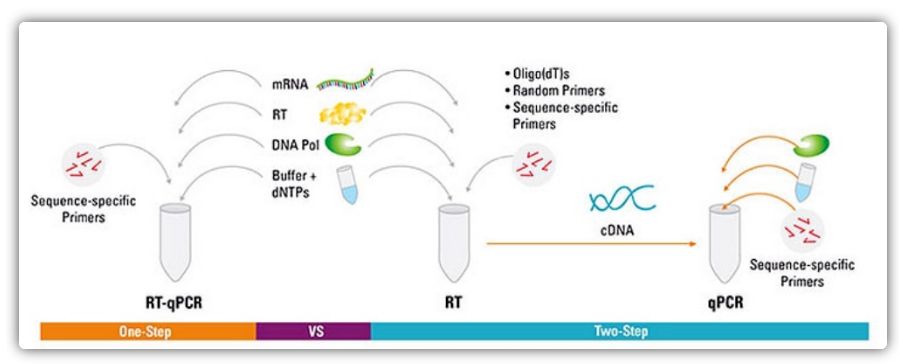
RT-qPCR kan opnås ved en et-trins eller to-trins metode.Et-trins RT-qPCR kombinerer revers transkription og PCR-amplifikation, hvilket tillader revers transkriptase og DNA-polymerase at fuldføre reaktionen i det samme rør under de samme bufferbetingelser.Et-trins RT-qPCR kræver kun brug af sekvensspecifikke primere.I to-trins RT-qPCR udføres revers transkription og PCR-amplifikation i to rør ved hjælp af forskellige optimerede buffere, reaktionsbetingelser og primerdesignstrategier.
| Fordel | Ulempe | |
| Et skridt | Denne metode har færre eksperimentelle fejl, da begge reaktioner udføres i et rør
Færre pipettering reducerer risikoen for kontaminering
Velegnet til high-throughput amplifikation/screening, hurtig og reproducerbar | To-trins reaktioner kan ikke optimeres separat
Da reaktionsbetingelserne kompromitteres ved at kombinere to-trins-reaktionen, er følsomheden ikke så god som for to-trins-metoden
Antallet af mål påvist af en enkelt prøve er lille |
| To trin | Evne til at skabe stabile cDNA-biblioteker, der kan opbevares i lange perioder og bruges i flere reaktioner
Målgener og referencegener kan amplificeres fra det samme cDNA-bibliotek uden behov for flere cDNA-biblioteker
Reaktionsbuffere og reaktionsbetingelser, der muliggør optimering af enkelte reaktionskørsler
Fleksibelt valg af triggerbetingelser | Brug af flere rør og flere pipetteringstrin øger risikoen for DNA-kontamination, og tidskrævende.
Kræver mere optimering end ettrinsmetoden |
Relaterede produkter:
RT-qPCR Easyᵀᴹ (One Step)-SYBR Grøn I
RT-qPCR Easyᵀᴹ (One Step)-Taqman
RT Easyᵀᴹ I Master Premix til første-strengs CDNA-syntese
Real Time PCR Easyᵀᴹ-SYBR Green I Kit
Udvælgelse af totalt RNA og mRNA
Når man designer et RT-qPCR-eksperiment, er det vigtigt at beslutte, om man vil bruge totalt RNA eller oprenset mRNA som skabelon til revers transkription.Selvom mRNA kan være i stand til at give lidt højere følsomhed, bruges total-RNA stadig hyppigt.Grunden til dette er, at total-RNA har en vigtigere fordel som udgangsmateriale end mRNA.For det første kræver processen færre oprensningstrin, hvilket sikrer bedre kvantitativ genvinding af skabelon og bedre normalisering af resultater til startcelletal.For det andet undgår den mRNA-berigelsestrinnet, som kan undgå muligheden for skæve resultater på grund af forskellige gendannelser af forskellige mRNA'er.Overordnet set, da den relative kvantificering af målgenet i de fleste anvendelser er vigtigere end den absolutte følsomhed af påvisningen, er total RNA mere egnet i de fleste tilfælde.
Revers transkriptionsprimer
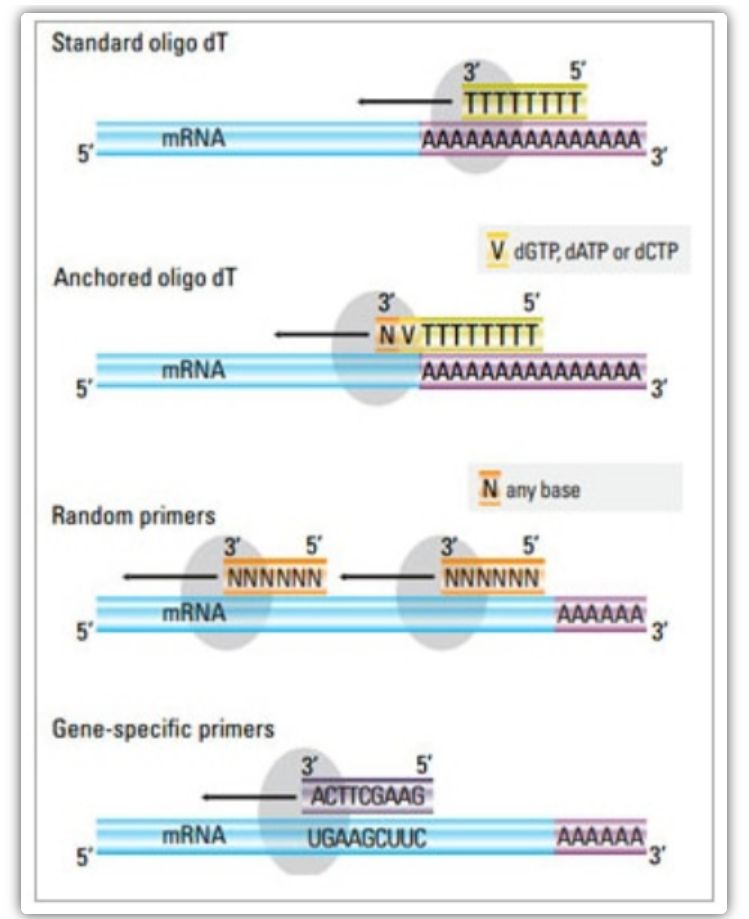
I to-trinsmetoden kan tre forskellige metoder anvendes til at prime cDNA-reaktionen: oligo(dT)-primere, tilfældige primere eller sekvensspecifikke primere.Typisk anvendes oligo(dT)-primere og tilfældige primere i kombination.Disse primere annealer til template-mRNA-strengen og giver revers transkriptase med et udgangspunkt for syntese.
| Primer valg | Struktur og funktion | Fordel | Ulempe |
| Oligo(dT) primer (eller forankret oligo(dT) primer) | Forlænget annealing til thyminrester ved poly(A)-halen af mRNA;ankeroligo(dT)-primer indeholder et G, C eller A i 3'-enden (ankersted) | Syntese af fuldlængde cDNA fra poly(A)-halet mRNA
Gælder, når mindre udgangsmateriale er tilgængeligt
Forankringsstedet sikrer, at oligo(dT)-primeren binder til 5′ poly(A)-halen af mRNA'et | Kun egnet til at amplificere gener med poly(A)-haler
Få cDNA trunkeret fra primingstedet*2 i poly(A)
Forspændt til at binde til 3′-enden*
*Denne mulighed minimeres, hvis der anvendes forankrede oligo(dT)-primere |
| tilfældig primer
| 6 til 9 baser i længden, som kan anneale til flere steder under RNA-transkription | Anneal til alle RNA'er (tRNA, rRNA og mRNA)
Velegnet til transskriptioner med betydelig sekundær struktur, eller når mindre udgangsmateriale er tilgængeligt
Højt cDNA-udbytte | cDNA er omvendt transskriberet fra alt RNA, hvilket normalt ikke er ønsket og kan fortynde signalet fra mål-mRNA'et
få trunkeret cDNA |
| sekvensspecifikke primere | Brugerdefinerede primere rettet mod specifikke mRNA-sekvenser | specifikt cDNA-bibliotek
Forbedre følsomheden
Brug af reverse qPCR-primere | Kun begrænset til syntesen af et enkelt målgen |
Omvendt transkriptase
Revers transkriptase er et enzym, der bruger RNA til at syntetisere DNA.Nogle reverse transkriptaser har RNase-aktivitet og kan nedbryde RNA-strenge i RNA-DNA-hybridstrenge efter transkription.Hvis det ikke har RNase-enzymatisk aktivitet, kan RNaseH tilføjes for højere qPCR-effektivitet.Almindeligt anvendte enzymer indbefatter Moloney murine leukæmivirus revers transkriptase og aviær myeloblastom virus revers transkriptase.For RT-qPCR er det ideelt at vælge en omvendt transkriptase med højere termostabilitet, så cDNA-syntese kan udføres ved højere temperaturer, hvilket sikrer vellykket transkription af RNA'er med højere sekundær struktur, samtidig med at deres fulde aktivitet opretholdes under hele reaktionen, hvilket resulterer i højere cDNA-udbytter.
Relaterede produkter:
Foreasy M-MLV omvendt transkriptase
RNase H-aktivitet af revers transkriptase
RNaseH er i stand til at nedbryde RNA-strenge fra RNA-DNA-duplekser, hvilket muliggør effektiv syntese af dobbeltstrenget DNA.Men når man bruger langt mRNA som skabelon, kan RNA'et blive nedbrudt for tidligt, hvilket resulterer i trunkeret cDNA.Derfor er det ofte fordelagtigt at minimere RNaseH-aktivitet under cDNA-kloning, hvis syntese af lange transkripter ønskes.I modsætning hertil er reverse transkriptaser med RNase H-aktivitet ofte gavnlige til qPCR-applikationer, fordi de øger smeltningen af RNA-DNA-duplekser under den første cyklus af PCR.
Primer design
PCR-primere, der anvendes til qPCR-trinnet i RT-qPCR, bør ideelt set designes til at spænde over en exon-exon-forbindelse, hvor en amplifikationsprimer potentielt kan spænde over en faktisk exon-intron-grænse.Da intron-holdige genomiske DNA-sekvenser ikke amplificeres, reducerer dette design risikoen for falske positiver amplificeret fra kontaminerende genomisk DNA.
Hvis primere ikke kan designes til at adskille exoner eller exon-exon-grænser, kan det være nødvendigt at behandle RNA-prøver med RNase-fri DNase I eller dsDNase for at fjerne genomisk DNA-kontamination.
RT-qPCR kontrol
En revers transkriptionsnegativ kontrol (-RT-kontrol) bør inkluderes i alle RT-qPCR-eksperimenter for at påvise DNA-kontamination (såsom genomisk DNA eller PCR-produkter fra tidligere reaktioner).Denne kontrol indeholder alle reaktionskomponenter undtagen revers transkriptase.Da revers transkription ikke forekommer med denne kontrol, hvis PCR-amplifikation observeres, er kontaminering fra DNA mest sandsynlig.
Indlægstid: Aug-02-2022








